FreePik
今回は、「ワクチンリスト解説 第7弾!」、アメリカ サンディエゴにある製薬会社のVicalが開発を進めている、VCL-HB01 というワクチンについての解説をしたいと思います。
以前も取り上げたことがあるので、その記事を見たい方は、こちらをクリックしてください。
まずは、Vicalさんのホームページは、こんな感じでございます… (^^♪
ちゃんとPipelineのところにも、「HSV2 VCL-HB01」とチャンと記載されておりますね☆
まずは一安心というところでしょうか… (^_-)-☆
ではでは、本題の VCL-HB01について簡単にこれまでのお話しをまとめてみることにしましょう。簡単なおさらいですね☆
まず、VCL-HB01についてですが、
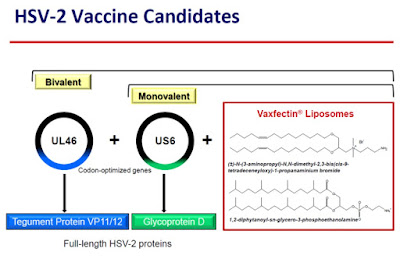
VCL-HB01はDNAワクチンの一種で、HSV2グリコプロテインD(gD)に対応するDNA(US6)と、外皮タンパク質UL46に対応するDNA(UL46)を組み込んだワクチンとなっており、Vcalが独自に開発した Vaxfectin を活性剤(アジュバント)として活用している
もののようでして、 ギニーピッグを使った治験Phase 1(動物実験)では、
- 感染部におけるウイルス複製を少なくすることができた
- 不活性状態でのウイルス感染を少なくすることができた
- 性器部分での発症およびウイルスの排出を有意に少なくすることができた
というような結果が得られているようです。
2017年に出された以下の論文で、最近の性感染症に対抗するためのワクチン研究についてまとめてあるものを見てみると…、(論文は以下のもの)
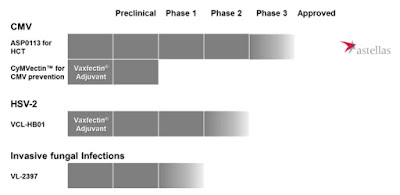
以前ご紹介したことのある、ワクチン開発の進捗状況を示す図が出ておりまして(下図参照)…

VCL-HB01の情報(一番上の左から三番目)については、
- 57% reduction in lesions but not shedding(病変の出現は57%減少、排出は減少なし)
- Reduction in HSV quantity(HSVの量に関しては減少)
と記述されておりました。
同論文中に記載されていたVCL-HB01に関する記述を見ると…、
Another candidate, VCL- HB01, is a DNA vaccine containing two codon optimized genes (gD2þVP11/12) with Vaxfectin adjuvant. In a Phase I/II study among HSV-2-seropositive people, VCL-HB01 did not meet the primary endpoint of decreased HSV shedding, but vaccine recipients had a 57% decrease in lesion frequency at 9 months and reduction in quantity of virus detected. The vaccine also induced UL46-specific T cell responses.
HSV2感染者に対するPhase 1/2の結果は、HSVの排出に関しては減少が見られなかったが、ワクチン接種後9か月目に測定した病変頻度に関しては57%減少しており、ウィルス量にも減少が見られた。また、同ワクチンにより UL46に対応したT細胞の反応も確認された。
といったようなことが書いてありまして…、
まあまあ期待できるかも…。これからに期待しましょう☆
という感じの印象を持ちました。
ちなみに、上記の結果は 2016年にVcalの研究者が学会で発表されているようでして…、その時の資料を見ると、「病変頻度(Lesion Frequency)が57%減少した」に関しては以下のようにまとめられていました。
実は、Phase 1/2の治験(人に対して行ったもの)では、
- グリコプロテインDに対応するDNA(US6)で作ったワクチン(赤色)
- US6と外皮タンパク質UL46に対応するDNA(UL46)で作ったワクチン(青色)
- 人体に無害の溶液(プラシボ)
の3種類でその効果を比較しているんですね。まぁ、この結果を見る限り…、
赤色・青色両方ともに病変の頻度も減っていて、特に9か月後の結果を見ると、2種類混合ワクチン(赤色)の方が良い結果が出ていて(57%減少)、なんかいい感じじゃないですか!
と思ったわけなんですが…、この表の結果をよく見ると…、
プラシボでも62%減少している… (;・∀・)
んですね…。
これは…、投稿するまでに色々と調べてみたんですが、
う~ん、分からん… (´・ω・`)
というのが本音でございます…。スミマセン、誰かお分かりになる方、教えて頂けないでしょうか…?力不足で申し訳ありませんが…、お願いします…。
ちなみに、このVCL-HB01に関しては、投資家を対象とした2017年Quatery Reportでは、以下のようなリスクを提示しています。
We initiated a Phase 2 clinical trial of VCL-HB01, our HSV-2 vaccine in September 2016, but the results of the Phase 2 clinical trial may not be positive and the favorable results or trends observed in our previously completed Phase 1/2 clinical trial may not continue in the Phase 2 clinical trial. The Phase 2 clinical trial of VCL-HB01 and any future trials, if any, may not demonstrate sufficient safety or efficacy to support further product development. Because we have a limited number of independent clinical-stage product candidates, if we experience a significant delay, set-back or failure in the development of any of our product candidates, it could have a material adverse impact on our business prospects.
Phase 1/2で得られたような良い結果がPhase 2でも見られるとは限らないのでご注意を…
まぁ、とりあえず、開発が続いているので安心ですが…、ちょっと結果の解釈(特にプラシボ群との比較)がよく分からないので…、
う~ん、ビミョーな感じ…
というのが今回感じたことです…。
まずは、今後の研究・治験結果に期待したいところですね☆(^^♪




0 件のコメント:
コメントを投稿